缺氧性肺动脉高压(HPH)并非简单的“肺部高血压”,它是机体长期处于低氧环境(如高原地区、慢性阻塞性肺疾病、间质性肺病、睡眠呼吸暂停等)时,肺部血管发生的一场危险重构。
研究数据触目惊心:HPH 患者的五年死亡率可高达40%,其死亡主因正是难以逆转的右心衰竭。即便当前有靶向肺血管舒张的药物(如内皮素受体拮抗剂、磷酸二酯酶-5抑制剂、前列环素类药物),它们虽能一定程度上缓解血管痉挛、降低肺动脉压力(约10-15%),但对已发生的肺血管结构重塑——即血管壁增厚、管腔狭窄的根本性病变,但效果甚微。

南京医科大学附属苏州医院等研究团队发表在《Scientific Reports》上的一项研究,揭示了间充质干细胞来源的外泌体(MSC-exo)在治疗低氧性肺动脉高压(HPH)中的关键作用。

为了验证 MSC-exo 对抗 HPH 的效力,研究团队进行了一系列严谨实验:
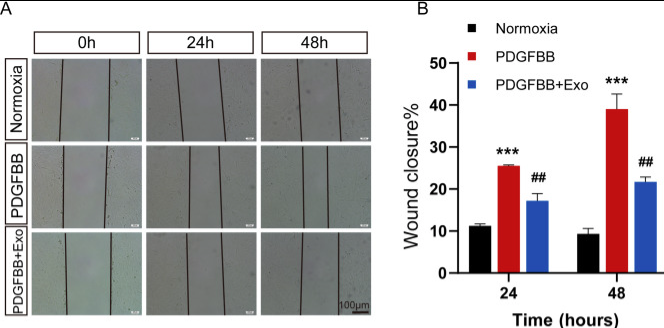
在体外实验中,科学家使用血小板衍生生长因子 BB(PDGF-BB)刺激肺动脉平滑肌细胞(PASMCs),成功模拟出 HPH 的细胞“失控”状态——细胞疯狂增殖和迁移。当引入MSC-exo后,这种异常行为被显著遏制。关键增殖标志物(PCNA, Ki67)表达下降,细胞划痕愈合速度减慢,证实 MSC-exo 能直接“驯服”病变的平滑肌细胞。
研究团队将大鼠置于模拟高原缺氧的环境(10%氧气,每天8小时,持续4周),成功诱导出典型的 HPH 表型:肺动脉压力(通过右心室收缩压 RVSP 测量)飙升、右心室肥厚、肺血管壁显著增厚、管腔狭窄。向这些患病大鼠静脉注射 MSC-exo 后,疗效令人振奋:与注射生理盐水的对照组相比,治疗组的 RVSP 显著回落,右心室肥厚程度减轻,肺小血管的壁厚和管壁面积明显缩小,血管重塑得到有效改善。更令人惊喜的是,肺组织内的纤维化程度(经 Masson 染色评估)也因 MSC-exo 的干预而减轻。
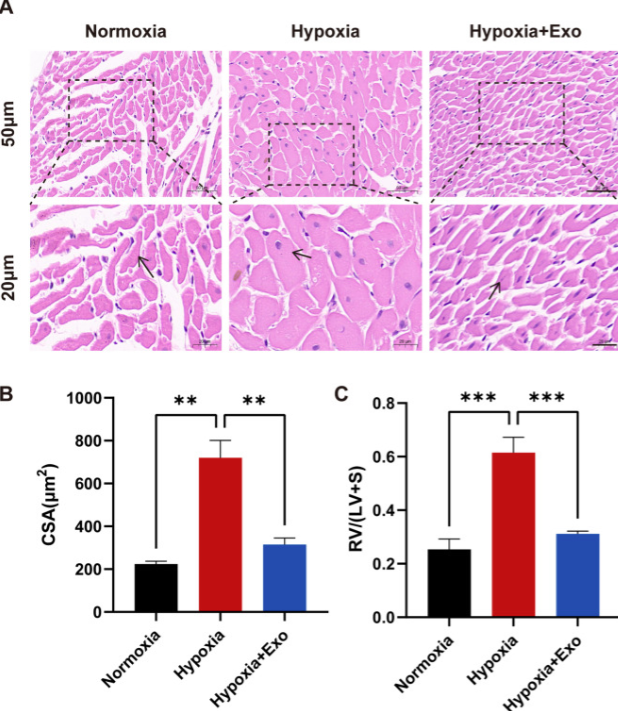
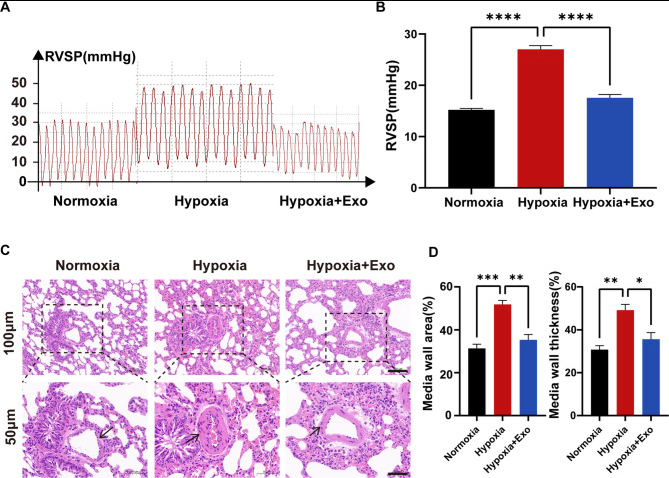
研究团队深入分子层面,揭示了其核心机制——精准“关闭”促重塑的 EGFR/ErbB2 异二聚体开关:
研究发现,在 PDGF-BB 刺激的 PASMCs 和 HPH 大鼠肺组织中,表皮生长因子受体(EGFR)和 ErbB2(一种原癌基因受体)的表达异常升高。更关键的是,两者频繁结合形成“异二聚体”(两个不同蛋白组成的复合体)。
这种异二聚体一旦形成,就如同启动了“增殖引擎”,强力激活下游的信号通路(如MAPK/ERK, PI3K/AKT),驱动 PASMCs 的异常增殖、迁移和生存,直接导致肺血管壁增厚、管腔狭窄——即血管重塑的核心过程。
实验证实,经 MSC-exo 处理后,病变细胞和组织中 EGFR 和 ErbB2 的表达水平被显著下调,更重要的是,两者形成异二聚体的能力被有效抑制。这如同切断了“增殖引擎”的点火开关,阻断了驱动肺血管重塑的核心信号流。研究还发现,低氧环境的核心调控因子 HIF-1α 可能参与上调了 EGFR/ErbB2 的表达,MSC-exo 可能也间接影响了这一上游调控。
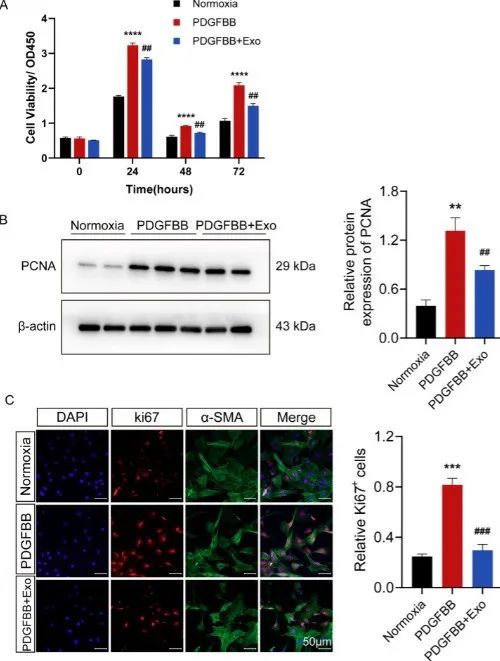
随着研究的深化和技术的进步,这些承载着生命修复密码的“天然纳米囊泡”,有望在未来成为临床医生手中对抗 HPH 的有力武器,为数百万深陷呼吸与心衰困境的患者重燃生命希望。
如需了解更多关于“肿瘤”信息
请与我们进一步联系







